Hay un tipo de paciente que probablemente reconoces en consulta: lleva meses —o años— con molestias abdominales recurrentes, hábitos intestinales impredecibles y una fatiga que no mejora con el descanso. Los estudios convencionales vuelven "normales". No hay patología estructural evidente. Y sin embargo, el paciente sigue incómodo o en sufrimiento.
Esta presentación clínica, más frecuente de lo que solemos reconocer, tiene un nombre: trastorno funcional gastrointestinal. Y en su centro, casi siempre, está el intestino.
El problema que no siempre nombramos
El Síndrome de Intestino Irritable (SII) es uno de los trastornos gastrointestinales funcionales más prevalentes y subestimados en la práctica clínica. Se caracteriza por dolor abdominal recurrente y alteraciones en los hábitos intestinales, con una prevalencia que oscila entre el 10 y el 25% en la población general, generando una carga significativa sobre la calidad de vida, la productividad laboral y el gasto en salud (Coda et al., 2023). A pesar de esta prevalencia, su diagnóstico sigue siendo un reto, pues se trata de un trastorno crónico sin anomalías estructurales ni bioquímicas identificables (Nathani & Shackelford, 2025).
Esto explica por qué muchos pacientes pasan años en un ciclo de consultas, pruebas y tratamientos sintomáticos sin una respuesta integradora. Y el SII no existe en aislamiento: estudios longitudinales muestran que más del 55% de los pacientes presentan solapamiento con dispepsia funcional, y que este grupo tiene síntomas más severos, con mayor prevalencia de ansiedad y depresión (Huang et al., 2023).
El eje intestino-cerebro: más que una metáfora
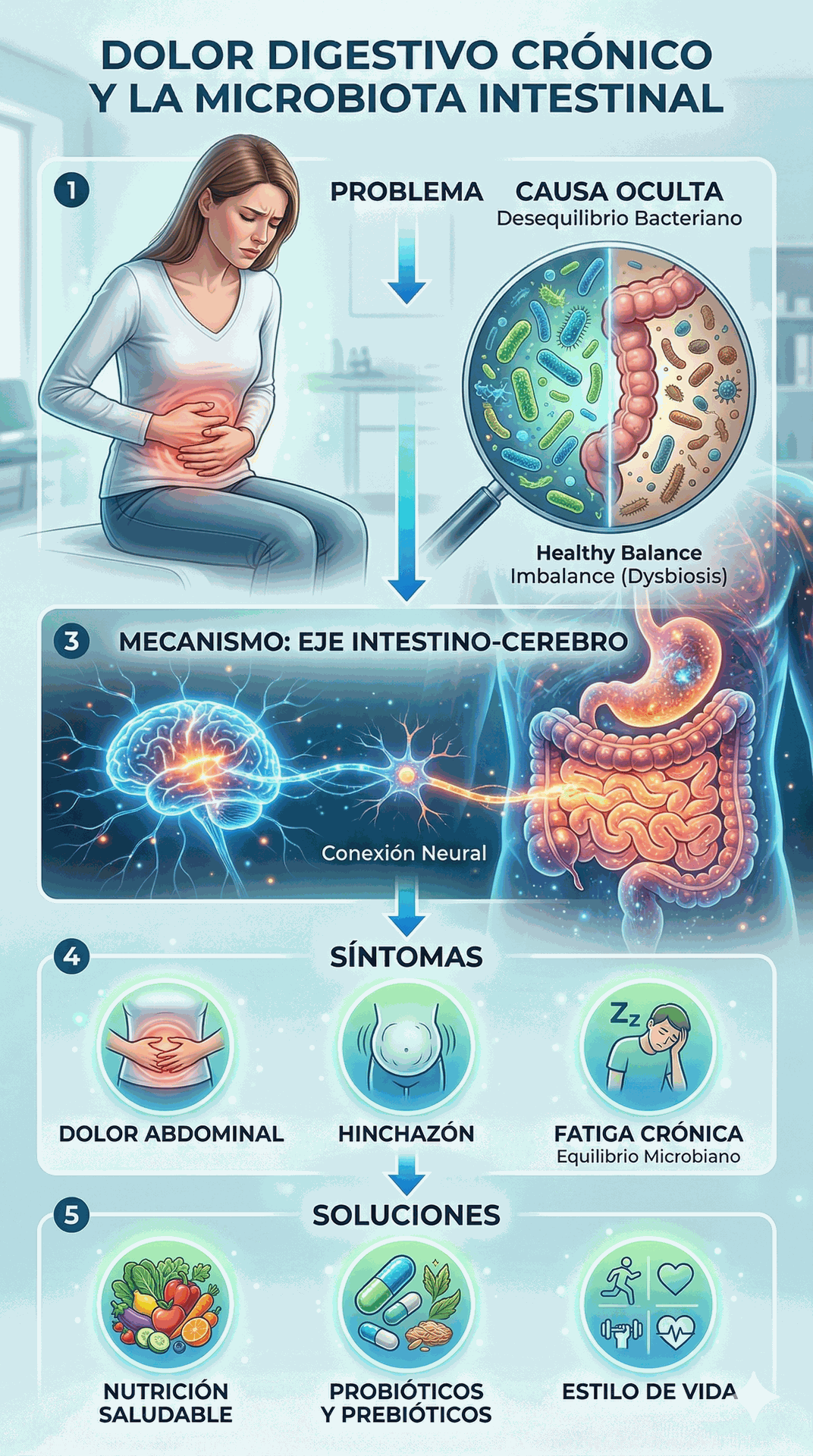
Para entender el SII y las intolerancias alimentarias asociadas, es fundamental dejar de ver el intestino como un órgano aislado. La fisiopatología del SII involucra una desregulación de la comunicación entre el cerebro y el intestino —el llamado eje intestino-cerebro— asociada con alteraciones en la motilidad intestinal, permeabilidad de la mucosa, hipersensibilidad visceral y la composición de la microbiota (Coda et al., 2023).
Uno de los mecanismos más relevantes en este eje es la permeabilidad intestinal aumentada. Cuando la barrera epitelial se compromete, productos microbianos como los lipopolisacáridos (LPS) ingresan a la circulación, activando el tejido linfoide asociado al intestino (GALT) y generando neuroinflamación que puede amplificar la percepción del dolor (Goudman et al., 2025). Esta cascada inflamatoria silenciosa es, en muchos casos, el sustrato detrás de los síntomas que el paciente describe como "intolerancia" a ciertos alimentos, dolor crónico o niebla mental.
La microbiota juega un papel central en esta comunicación: sus interacciones con células inmunes, células enterocromafines y mediadores luminales conforman un modelo integrativo del eje microbiota-intestino-cerebro, con interacciones recíprocas entre redes cerebrales y redes intestinales (Kucharzik et al., 2024).
Intolerancias: entre la percepción y la fisiopatología
Las intolerancias alimentarias en el contexto del SII son frecuentemente subestimadas o mal clasificadas. No siempre implican un mecanismo inmunomediado clásico (IgE), pero eso no las hace menos reales. Los carbohidratos fermentables —FODMAPs— han sido los más estudiados como desencadenantes de síntomas: la evidencia muestra que los carbohidratos de cadena corta y alta fermentabilidad incrementan la producción de gas colónico y el volumen de agua en el intestino delgado, exacerbando los síntomas en pacientes susceptibles (Sarvepalli et al., 2023).
El gluten también ocupa un lugar relevante en esta conversación. Aunque la enfermedad celíaca es un diagnóstico diferencial obligado, existe evidencia de sensibilidad al gluten no celíaca en pacientes con SII. Un ensayo controlado demostró que el 68% de los pacientes experimentaron agravamiento de síntomas al reintroducir gluten, en comparación con el 40% del grupo placebo, aunque sin un mecanismo fisiopatológico completamente elucidado (Sarvepalli et al., 2023).
Del síntoma al abordaje: lo que la evidencia respalda
La intervención dietaria ya no es una recomendación de segundo orden. Las guías actualizadas de la British Gastroenterological Society (2021) y el American College of Gastroenterology (2022) posicionan el asesoramiento dietético como una opción de primera línea en el manejo del SII (Huang et al., 2023).
Más allá de las dietas de eliminación, el abordaje integrativo ha mostrado resultados prometedores. Intervenciones basadas en nutrición han logrado reducciones estadísticamente significativas de los síntomas gastrointestinales en pacientes con SII en todas sus variantes —con predominio de estreñimiento, diarrea y hábito mixto—, con mejoras sostenidas en los puntajes clínicos de síntomas (Carone et al., 2024).
El manejo efectivo del SII requiere entonces una mirada multidimensional: historia clínica detallada, evaluación de patrones alimentarios, consideración del eje emocional-intestinal y, cuando sea pertinente, protocolos de reintroducción estructurados que permitan identificar desencadenantes individuales.
El intestino como punto de partida
El dolor crónico digestivo, las intolerancias y el SII no son diagnósticos de exclusión que se entregan como último recurso. Son entidades clínicas con fisiopatología cada vez mejor comprendida, que responden a intervenciones concretas cuando se abordan con criterio.
Como profesionales de la salud, se tiene la oportunidad —y la responsabilidad— de generar conciencia en los pacientes: el intestino no solo digiere alimentos. Regula la inflamación, modula el dolor, influencia el estado de ánimo y se comunica constantemente con el cerebro. Cuidarlo es cuidar al paciente en su totalidad.
Si este tipo de pacientes es frecuente en tu consulta, quizás el siguiente paso no es pedir más estudios, sino empezar a mirar el intestino desde una perspectiva funcional y basada en microbiota. Contáctanos a través de este link
Referencias
- Carone, L., et al. (2024). Treatment of functional bowel disorders in an integrative medicine clinic. JGH Open. https://doi.org/10.1002/jgh3.13042
- Coda, S., et al. (2023). IBS and the Gut Microbiome: A Comprehensive Review. J Clin Med, 12(7), 2558. https://doi.org/10.3390/jcm12072558
- Goudman, L., et al. (2025). The brain-gut axis and chronic pain: mechanisms and therapeutic opportunities. Front Neurosci. https://doi.org/10.3389/fnins.2025.1545997
- Huang, K.Y., et al. (2023). Irritable bowel syndrome: Epidemiology, overlap disorders, pathophysiology and treatment. World J Gastroenterol, 29(26), 4120–4135. https://doi.org/10.3748/wjg.v29.i26.4120
- Kucharzik, T., et al. (2024). Intestinal Permeability in Disorders of Gut–Brain Interaction: From Bench to Bedside. Gastroenterology. https://doi.org/10.1053/j.gastro.2024.08.032
- Nathani, R.R., & Shackelford, K.B. (2025). Irritable Bowel Syndrome. StatPearls. https://www.ncbi.nlm.nih.gov/books/NBK534810/
- Sarvepalli, S., et al. (2023). Digesting the Impact of Diet on IBS. Cureus, 15(9), e45279. https://doi.org/10.7759/cureus.45279
