El descubrimiento que cambió la forma de entender el riesgo cardiovascular
Durante décadas, cuando pensábamos en salud cardiovascular, la fórmula parecía simple: controla tu colesterol, haz ejercicio, no fumes, mantén tu presión arterial bajo control. Pero había un problema: muchos pacientes hacían todo "correctamente" y aun así desarrollaban enfermedad cardíaca. Otros, con factores de riesgo alarmantes, parecían inexplicablemente protegidos. Faltaba una pieza del rompecabezas.
Esa pieza estaba a metros de distancia del corazón: en el intestino.
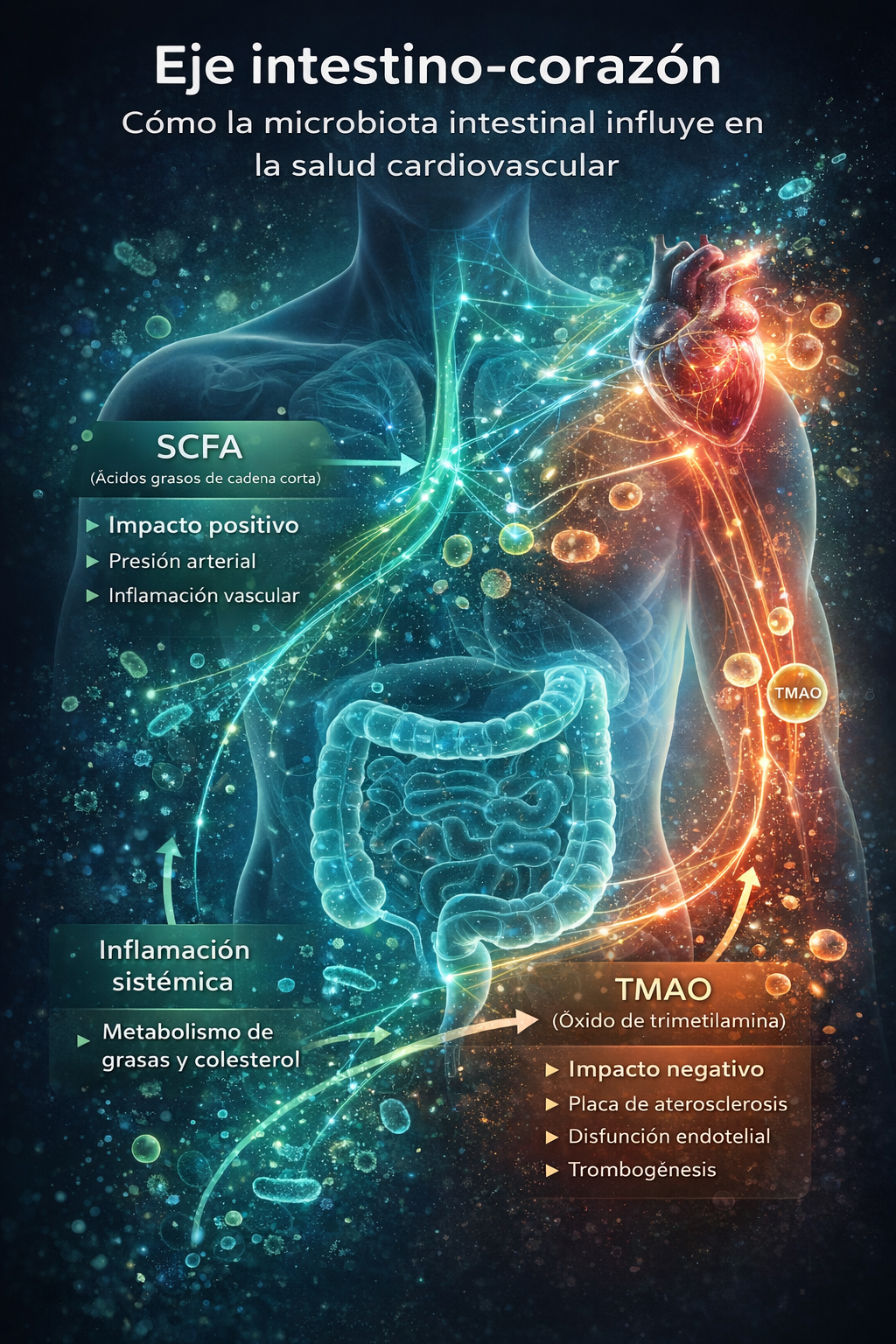
Investigaciones recientes han revelado algo sorprendente: las bacterias que habitan nuestro tracto digestivo no solo influyen en nuestra digestión, sino que están enviando constantemente señales químicas que afectan directamente la salud de nuestras arterias, la presión arterial, la formación de coágulos y el riesgo de infarto. Esta conexión, conocida como el eje intestino-corazón, representa una de las fronteras más emocionantes de la medicina cardiovascular moderna.
Los números hablan por sí solos. Las enfermedades cardiovasculares siguen siendo la primera causa de muerte a nivel global, pero ahora sabemos que la composición de nuestra microbiota intestinal puede predecir el riesgo cardiovascular independientemente de los factores tradicionales (Nesci et al., 2023). Más importante aún: la evidencia sugiere que podemos modificar esa microbiota y, con ello, nuestro destino cardiovascular.
El eje intestino-corazón: cómo la microbiota se comunica con el sistema cardiovascular
Imagina que tus bacterias intestinales son una fábrica química funcionando las 24 horas del día. Procesan todo lo que comemos y producen cientos de moléculas diferentes que entran al torrente sanguíneo y viajan por todo el cuerpo, incluyendo el corazón y arterias. Algunas de estas moléculas son protectoras, otras son dañinas, y el balance entre ambas puede marcar la diferencia entre salud y enfermedad.
La microbiota intestinal se comunica con el sistema cardiovascular a través de múltiples vías interconectadas. Produce metabolitos que pueden inflamar o proteger el revestimiento de las arterias, modula cómo el hígado procesa el colesterol, influye en la presión arterial a través del sistema nervioso, y regula la capacidad de coagulación de la sangre (Massey et al., 2022). Esta red de comunicación bidireccional es tan poderosa que los investigadores ahora hablan del "eje intestino-corazón" como un sistema integrado.
Estudios recientes han identificado perfiles específicos de disbiosis intestinal (desequilibrio microbiano) asociados con diferentes tipos de enfermedad cardiovascular. Pacientes con atherosclerosis avanzada muestran patrones microbianos distintos a aquellos con hipertensión o insuficiencia cardíaca, sugiriendo que la microbiota no solo influye en el riesgo general sino también en cómo se manifiesta la enfermedad cardiovascular (Alexandrescu et al., 2024).
TMAO: un metabolito clave en el riesgo cardiovascular
Entre los metabolitos derivados de la microbiota intestinal, el óxido de trimetilamina (TMAO) se ha consolidado en la última década como uno de los biomarcadores emergentes más estudiados en la fisiopatología de la enfermedad cardiovascular. La evidencia acumulada sugiere que no se trata únicamente de un marcador metabólico, sino de un mediador potencialmente activo en la progresión de la aterosclerosis.
El TMAO se genera a partir de un proceso metabólico dependiente de la interacción microbiota–hospedero. Nutrientes dietarios como la colina, la fosfatidilcolina y la L-carnitina —presentes principalmente en carnes rojas, yema de huevo y algunos pescados— son metabolizados por bacterias intestinales en trimetilamina (TMA). Posteriormente, esta molécula es absorbida y oxidada en el hígado por enzimas del sistema flavina monooxigenasa (principalmente FMO3), generando TMAO, que pasa a la circulación sistémica.
Diversos estudios han demostrado que el TMAO participa en múltiples mecanismos implicados en la aterogénesis. A nivel celular, favorece la formación de células espumosas al modular la captación de colesterol por macrófagos, altera el transporte reverso de colesterol y promueve la disfunción endotelial. Adicionalmente, se ha asociado con la activación de vías inflamatorias, incluyendo el inflamasoma NLRP3, así como con un aumento en la reactividad plaquetaria, lo que contribuye a un mayor riesgo trombótico (Zhen et al., 2023; Dolkar et al., 2024).
La relevancia clínica de este metabolito ha sido respaldada por estudios en cohortes humanas. Investigaciones longitudinales, incluyendo datos del Framingham Heart Study, han mostrado que concentraciones elevadas de TMAO se asocian con mayor incidencia de eventos cardiovasculares mayores —como infarto de miocardio, accidente cerebrovascular y mortalidad cardiovascular— independientemente de factores de riesgo tradicionales (Witkowski et al., 2020). Asimismo, metaanálisis recientes han reforzado la hipótesis de que el TMAO podría desempeñar un papel activo en la progresión de la enfermedad cardiovascular (Hassan et al., 2023).
Un aspecto particularmente relevante desde la perspectiva de medicina personalizada es la variabilidad interindividual en la producción de TMAO.
Incluso con patrones dietarios similares, las concentraciones plasmáticas pueden variar significativamente entre individuos, lo que refleja diferencias en la composición y actividad metabólica de la microbiota intestinal. Este fenómeno sugiere que el perfil microbiano podría modular la respuesta metabólica a determinados nutrientes, abriendo nuevas oportunidades para la estratificación de riesgo cardiovascular basada en microbioma.
Ácidos grasos de cadena corta (SCFA): metabolitos protectores
En contraste con metabolitos asociados a mayor riesgo cardiovascular, como el TMAO, los ácidos grasos de cadena corta (SCFA) representan uno de los principales mecanismos a través de los cuales la microbiota intestinal ejerce efectos protectores sobre la salud metabólica y cardiovascular.
Los SCFA —principalmente acetato, propionato y butirato— se producen a partir de la fermentación bacteriana de fibra dietaria no digerible proveniente de alimentos como frutas, vegetales, legumbres y cereales integrales. Estas moléculas actúan como mediadores metabólicos y señalizadores inmunológicos que influyen en múltiples procesos fisiológicos relevantes para la homeostasis cardiovascular.
A nivel vascular e inmunológico, los SCFA activan receptores acoplados a proteína G, particularmente GPR41 y GPR43, que participan en la modulación de respuestas inflamatorias y en la regulación del tono vascular (Manolis et al., 2022; Singh et al., 2024). Esta interacción explica, en parte, la asociación observada entre dietas ricas en fibra y un mejor control de la presión arterial.
El butirato, uno de los SCFA más estudiados, presenta además efectos importantes sobre la integridad de la barrera intestinal. Al fortalecer las uniones estrechas del epitelio intestinal, reduce la translocación de endotoxinas bacterianas como el lipopolisacárido (LPS), disminuyendo así la inflamación sistémica de bajo grado asociada con enfermedad cardiometabólica.
Adicionalmente, el butirato promueve la diferenciación de células T reguladoras, contribuyendo a la regulación de la respuesta inmune.
Desde el punto de vista metabólico y epigenético, el butirato también actúa como inhibidor de histona deacetilasas (HDAC), modulando la expresión génica en diferentes tejidos. Estudios recientes sugieren que este mecanismo podría influir en vías metabólicas hepáticas relacionadas con la producción de TMAO, lo que plantea una interacción funcional entre metabolitos microbianos potencialmente perjudiciales y aquellos con efectos protectores (Alexandrescu et al., 2024; Gan et al., 2024).
En este contexto, el equilibrio entre metabolitos derivados de la microbiota —como TMAO y SCFA— ha emergido como un eje regulador clave en la fisiopatología de la enfermedad cardiovascular. Evidencia epidemiológica respalda esta relación: poblaciones con patrones dietarios ricos en fibra fermentable, como la dieta mediterránea, presentan mayores niveles de SCFA y menor riesgo de eventos cardiovasculares (Rinott et al., 2021). Asimismo, intervenciones dietarias orientadas a aumentar la ingesta de fibra han demostrado mejoras en la presión arterial y otros biomarcadores cardiometabólicos, en parte mediadas por el aumento en la producción de SCFA (Verhaar et al., 2020).
Evidencia clínica: lo que muestran los estudios en humanos
La conexión entre microbiota y enfermedad cardiovascular no es solo teórica o basada en modelos animales. Múltiples estudios en humanos han confirmado estos hallazgos en poblaciones reales. Un análisis comparativo mostró que pacientes con aterosclerosis sintomática presentaban mayor abundancia de bacterias del género Collinsella y menor presencia de bacterias productoras de butirato; además, sus comunidades microbianas tenían mayor capacidad funcional para producir TMAO y menor capacidad de fermentación de fibra (Tang et al., 2017). De manera consistente, un estudio prospectivo con más de 1,200 participantes encontró que quienes tenían niveles de TMAO en el cuartil más alto presentaban un riesgo 2.5 veces mayor de eventos cardiovasculares adversos, incluso tras ajustar por factores de riesgo tradicionales (Witkowski et al., 2019).
Estudios de intervención también apoyan un papel causal de la microbiota. La suplementación con colina o carnitina incrementó significativamente el TMAO solo en individuos con microbiota productora de TMA, mientras que la supresión temporal de la microbiota con antibióticos redujo casi por completo su producción (Tang et al., 2013). En contraste, estudios poblacionales han mostrado que una mayor ingesta de fibra se asocia con menor riesgo cardiovascular, mediado en parte por mayores niveles de ácidos grasos de cadena corta (SCFA), particularmente butirato, los cuales se han relacionado con mejor control de la presión arterial y menor rigidez arterial (Verhaar et al., 2020).
Estrategias para modular la microbiota y proteger el corazón
Comprender la conexión entre microbiota y salud cardiovascular es fascinante, pero la pregunta crucial es: ¿qué podemos hacer al respecto?
- Intervenciones dietéticas constituyen la primera línea de acción para modular metabolitos derivados de la microbiota. Reducir el consumo de carnes rojas y alimentos ricos en colina puede disminuir significativamente los niveles de TMAO; por ejemplo, un estudio mostró que reducir la ingesta de carne roja de 180 g a menos de 60 g diarios se asoció con una disminución del 30–40% en TMAO circulante en cuatro semanas (Abrignani et al., 2024). Paralelamente, aumentar la ingesta de fibra —como en la dieta mediterránea— favorece bacterias productoras de butirato como Faecalibacterium prausnitzii y Akkermansia muciniphila, con beneficios sobre la microbiota y marcadores cardiometabólicos (Rinott et al., 2021).
- Probióticos y prebióticos representan una estrategia complementaria para modular la microbiota. Cepas de Bifidobacterium y Lactobacillus han mostrado mejorar el perfil lipídico en estudios clínicos, mientras que microorganismos emergentes como Akkermansia muciniphila se investigan por su efecto en la integridad de la barrera intestinal y el metabolismo lipídico (Verhaar et al., 2020). Un metaanálisis reportó que la suplementación con probióticos y simbióticos se asocia con reducción de TMAO, mejora del perfil lipídico y disminución de marcadores inflamatorios y de disfunción endotelial como ICAM-1 (Haghighat et al., 2019).
- Inhibidores de TMA líasa representan un enfoque farmacológico novedoso. Estas moléculas bloquean las enzimas bacterianas que convierten colina y carnitina en TMA, cortando la producción de TMAO en su origen. Estudios preclínicos han mostrado que estos inhibidores pueden reducir niveles de TMAO hasta en 95% y prevenir la progresión de aterosclerosis en modelos animales (Cai et al., 2022). Actualmente hay ensayos clínicos en fase II evaluando la seguridad y eficacia de estos compuestos en humanos.
Microbiota y medicina cardiovascular de precisión
La evidencia reciente sugiere que la microbiota intestinal desempeña un papel relevante en la fisiopatología de la enfermedad cardiovascular, abriendo la puerta a un enfoque de medicina de precisión basado en el perfil microbiano de cada paciente. En este contexto, el análisis funcional de la microbiota podría complementar los factores de riesgo tradicionales, permitiendo identificar diferencias metabólicas entre pacientes que influyen en su riesgo cardiovascular.
Por ejemplo, algunos individuos presentan una mayor capacidad microbiana para producir trimetilamina (TMA), posteriormente, TMAO, y eventos cardiovasculares. En contraste, otros pueden tener una menor presencia de bacterias productoras de ácidos grasos de cadena corta (SCFA). Estas diferencias podrían orientar intervenciones más personalizadas, desde recomendaciones nutricionales específicas hasta estrategias dirigidas a modular la microbiota.
En conjunto, estos hallazgos reflejan un cambio de paradigma: la salud cardiovascular no depende únicamente de factores tradicionales, sino también de la interacción entre dieta, microbiota y metabolitos microbianos. Comprender este eje intestino-corazón podría ampliar las estrategias de prevención y manejo del riesgo cardiometabólico en la práctica clínica.
Referencias científicas
- Abrignani, M. G., Luca, F., Favilli, S., et al. (2024). Dietary interventions to lower TMAO and cardiovascular risk. American Journal of Clinical Nutrition, 119(2), 324-332.
- Alexandrescu, A., Grigore, M., & Anghel, L. (2024). Gut microbiota regulate atherosclerosis via the gut-vascular axis. Frontiers in Microbiology, 15, 1606309.
- Cai, T., Zheng, Y., Wang, H., et al. (2022). TMA lyase inhibitors as a novel therapeutic strategy for cardiovascular disease. Cardiovascular Research, 118(5), 1245-1258.
- Dolkar, P., Singh, R., & Kumar, A. (2024). TMAO and atherosclerotic plaque instability: mechanisms and clinical implications. Atherosclerosis, 389, 117425.
- Gan, X., Zhang, L., Liu, Y., et al. (2024). Fecal microbiota transplantation attenuates atherosclerosis by modulating gut-heart axis. Circulation Research, 134(8), 1024-1038.
- Hassan, D., Zahra, T., Kanaan, G., et al. (2023). The impact of gut microbiome constitution to reduce cardiovascular disease risk: A systematic review and meta-analysis. Current Problems in Cardiology, 48(3), 101459.
- Haghighat, N., Rajabi, S., & Mohammadshahi, M. (2019). Effect of synbiotic supplementation on cardiovascular risk factors in hemodialysis patients. Nephrology Dialysis Transplantation, 34(6), 1028-1035.
- Manolis, A. A., Manolis, T. A., Manolis, A. S., et al. (2022). Short-chain fatty acids and cardiovascular disease. International Journal of Cardiology, 355, 172-179.
- Massey, W., Brown, J. M., & Hazen, S. L. (2022). Gut microbiota-derived metabolites in cardiovascular health and disease. Current Atherosclerosis Reports, 24(5), 309-324.
- Nesci, A., Carnuccio, C., Ruggieri, V., et al. (2023). Gut microbiota and cardiovascular disease: evidence on the metabolic and inflammatory background of a complex relationship. International Journal of Molecular Sciences, 24(10), 9087.
- Rinott, E., Meir, A. Y., Tsaban, G., et al. (2021). The effects of the Green-Mediterranean diet on cardiometabolic health are linked to gut microbiome modifications: a randomized controlled trial. Genome Medicine, 13, 29.
- Singh, R., Zogg, H., & Ghoshal, U. C. (2024). Gut microbiota on cardiovascular diseases: current evidence and therapeutic potential. Frontiers in Cardiovascular Medicine, 11, 1572948.
- Tang, W. H. W., Kitai, T., & Hazen, S. L. (2017). Gut microbiota in cardiovascular health and disease. Circulation Research, 120(7), 1183-1196.
- Tang, W. H. W., Wang, Z., Levison, B. S., et al. (2013). Intestinal microbial metabolism of phosphatidylcholine and cardiovascular risk. New England Journal of Medicine, 368(17), 1575-1584.
- Verhaar, B. J. H., Collard, D., Prodan, A., et al. (2020). Associations between gut microbiota, faecal short-chain fatty acids, and blood pressure across ethnic groups: the HELIUS study. European Heart Journal, 41(44), 4259-4267.
- Witkowski, M., Weeks, T. L., & Hazen, S. L. (2020). Gut microbiota and cardiovascular disease. Circulation Research, 127(4), 553-570.
- Witkowski, M., Nemet, I., & Hazen, S. L. (2019). Trimethylamine N-oxide predicts cardiovascular mortality in peripheral artery disease. Scientific Reports, 9(1), 15580.
- Zhang, L., Gan, X., Liu, Y., et al. (2025). Fecal microbiota transplantation regulates gut-vascular axis in atherosclerosis. Cell Host & Microbe, 33(1), 18-32.
- Zhen, J., Zhou, Z., He, M., et al. (2023). The gut-heart axis: molecular mechanisms of atherosclerosis mediated by the gut microbiota. Nutrients, 15(16), 3645.
Artículo técnico elaborado por el equipo científico de Astrolab Bio.
