Muchos pacientes consultan por síntomas persistentes como distensión abdominal, fatiga o manifestaciones cutáneas sin un diagnóstico claro. A pesar de múltiples estudios, los resultados suelen ser normales.
Aquí es donde surge una hipótesis cada vez más respaldada por la evidencia:
¿y si el problema no está en lo que medimos… sino en la integridad de la barrera intestinal?
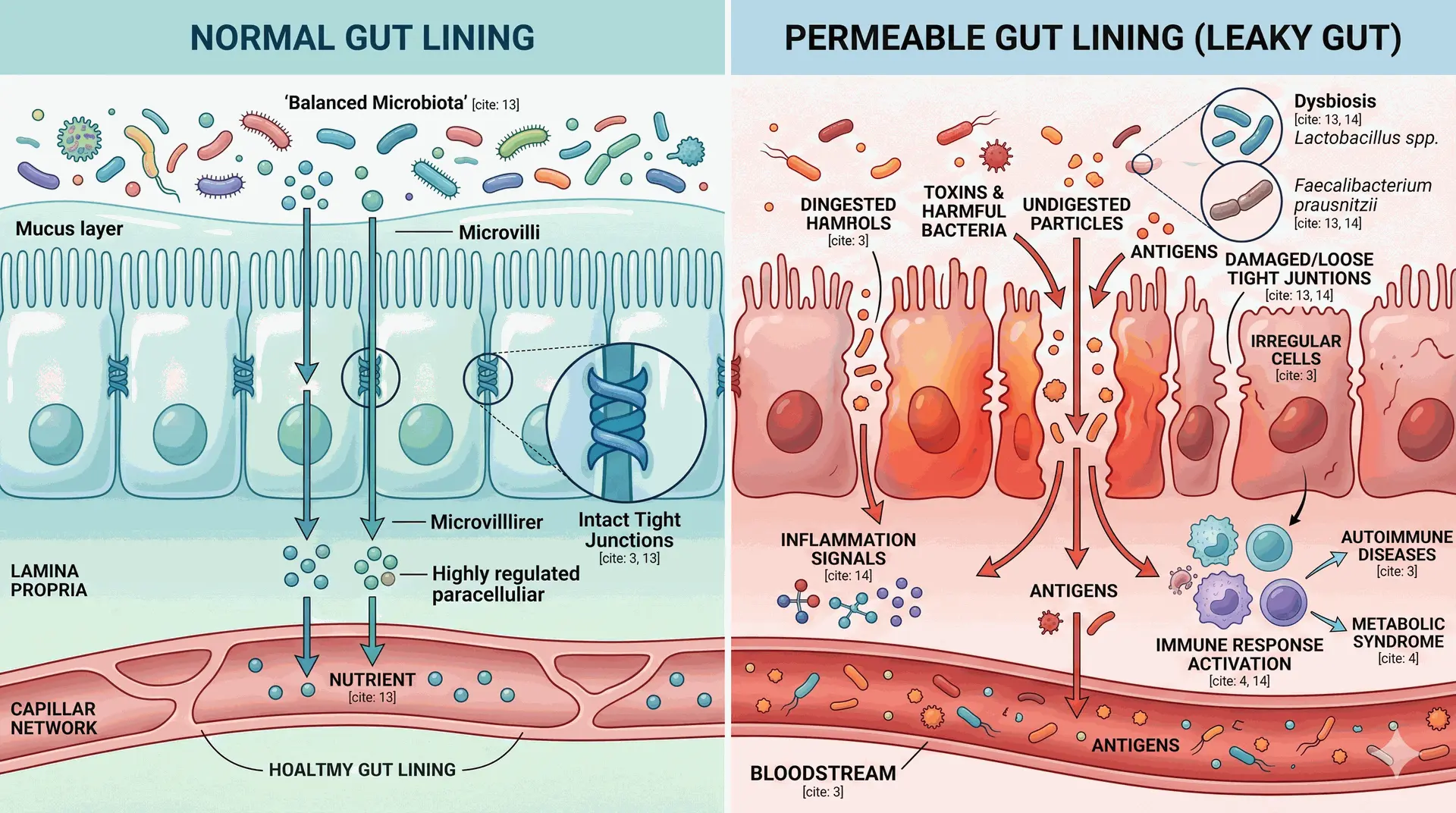
La permeabilidad intestinal aumentada (PIA) permite el paso de toxinas, antígenos y fragmentos bacterianos al torrente sanguíneo, activando procesos inflamatorios sistémicos de bajo grado.
Contexto clínico y fisiopatología relevante
El término intestino permeable se refiere a la disfunción de las uniones estrechas (tight junctions) del epitelio intestinal que permite el pasaje paracelular de antígenos luminales, lipopolisacáridos (LPS) y fragmentos bacterianos hacia la circulación sistémica. Este proceso activa respuestas inmunes de bajo grado sostenidas en el tiempo, con implicancias demostradas en enfermedades autoinmunes, síndrome metabólico y alteraciones neuropsiquiátricas.[1,2]
La zonulina es actualmente el biomarcador más validado para evaluar la integridad de dichas uniones. Su elevación en suero o materia fecal permite objetivar la permeabilidad intestinal aumentada (PIA) más allá del cuadro sintomático, y constituye un punto de referencia para monitorizar la respuesta al tratamiento.[3]
Presentación del caso
Perfil de la paciente
Mujer de 34 años, docente, sin antecedentes patológicos de relevancia. Consultó por primera vez por distensión abdominal crónica, fatiga persistente que interfería con sus actividades laborales, erupciones cutáneas recurrentes sin causa dermatológica confirmada y dificultad de concentración (referida como "niebla mental"). El cuadro llevaba 18 meses de evolución y había sido evaluado en múltiples consultas previas sin resultado diagnóstico concluyente.
Evaluación diagnóstica
Se solicitó perfil de permeabilidad intestinal que incluyó: zonulina en heces (resultado: 180 ng/mL; referencia < 100 ng/mL), análisis de microbiota por secuenciación 16S rRNA —con hallazgo de disbiosis caracterizada por reducción de Lactobacillus spp. y Faecalibacterium prausnitzii—, proteína C reactiva de alta sensibilidad (PCR-hs: 4.2 mg/L) e IgG alimentario para trigo y lácteos, ambos elevados.[4]
Intervención: protocolo de 12 semanas
|
Sem. 1–2 Remoción |
Eliminación de gluten, lácteos, alcohol, azúcares refinados y aditivos industriales (emulsionantes, carragenano). Reducción de AINEs tras consulta con médico tratante. |
|
Sem. 3–6 Reparación |
L-glutamina 5 g/día en ayunas. Zinc carnosina 75 mg/día. Vitamina D3 4.000 UI/día (basal: 18 ng/mL). Incorporación de caldo de huesos 2–3 veces por semana. |
|
Sem. 5–10 Resiembra |
Probióticos multicepa: L. rhamnosus GG + B. longum BB536, 20×10⁹ UFC/día. Prebióticos (inulina + FOS) 5 g/día progresivo. Dieta alta en fibra fermentable. |
|
Sem. 10–12 Reintroducción |
Reintroducción gradual y monitoreada. Registro sintomático por la paciente. Exclusión definitiva de gluten confirmada por respuesta clínica. |
Resultados al cierre del seguimiento
|
Parámetro / Síntoma |
Basal |
Semana 12 |
|
Zonulina fecal |
180 ng/mL ↑ |
89 ng/mL ✓ |
|
PCR de alta sensibilidad |
4.2 mg/L ↑ |
1.1 mg/L ✓ |
|
Distensión abdominal (EVA) |
8/10 |
2/10 |
|
Fatiga / brain fog |
Diaria, incapacitante |
Ocasional, manejable |
|
Erupciones cutáneas |
Frecuentes (2–3/semana) |
Resueltas desde sem. 6 |
La remisión de las erupciones cutáneas fue evidente desde la semana 6, coincidiendo con la fase de resiembra de microbiota. La paciente refirió mejoría progresiva del sueño y recuperación del rendimiento cognitivo, sin efectos adversos asociados al protocolo. Durante la fase de reintroducción, la respuesta clínica confirmó intolerancia persistente al gluten, por lo que se mantuvo la exclusión de forma indefinida con control semestral programado.[5]
Consideraciones para la práctica clínica
Este caso ilustra la utilidad de un abordaje secuencial y bien documentado frente a la PIA. Lo que con frecuencia llega a consulta como un cuadro difuso e inespecífico puede resolverse cuando se cuenta con biomarcadores adecuados y un plan de intervención estructurado. La evidencia disponible respalda el uso de la zonulina como marcador de seguimiento, la eficacia de probióticos de cepa documentada y el rol central de la L-glutamina en la reparación epitelial.
Sin embargo, la heterogeneidad de los estudios existentes exige prudencia cuando se trata de extrapolar resultados individuales a protocolos generales. Se recomienda evaluar cada caso con perfil de biomarcadores completo antes de iniciar la intervención, documentar la evolución con escalas validadas y considerar el abordaje interdisciplinario —gastroenterología, nutrición clínica, inmunología— en pacientes con comorbilidades autoinmunes asociadas.
Este tipo de casos plantea una pregunta clave para la práctica clínica:
¿cuántos pacientes con síntomas persistentes podrían beneficiarse de una evaluación más profunda de su microbiota intestinal?
REFERENCIAS
[1] Fasano A. Leaky gut and autoimmune diseases. Clin Rev Allergy Immunol. 2012;42(1):71–78. doi:10.1007/s12016-011-8291-x
[2] Bischoff SC, et al. Intestinal permeability — a new target for disease prevention and therapy. BMC Gastroenterol. 2014;14:189. doi:10.1186/s12876-014-0189-7
[3] Fasano A. Zonulin and its regulation of intestinal barrier function: the biological door to inflammation, autoimmunity, and cancer. Physiol Rev. 2011;91(1):151–175. doi:10.1152/physrev.00003.2008
[4] Lerner A, Matthias T. Changes in intestinal tight junction permeability associated with industrial food additives explain the rising incidence of autoimmune disease. Autoimmun Rev. 2015;14(6):479–489. doi:10.1016/j.autrev.2015.01.009
[5] Camilleri M. Leaky gut: mechanisms, measurement and clinical implications in humans. Gut. 2019;68(8):1516–1526. doi:10.1136/gutjnl-2019-318427
